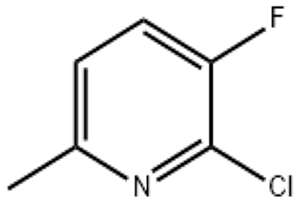
2-kloro-3-fluoro-6-pikolin(CAS št. 374633-32-6)
Uvod
Videz: Običajno brezbarvna do svetlo rumena tekočina, te značilnosti videza pomenijo, da je lahko občutljiva na svetlobo in toploto, zato je treba sprejeti ukrepe za izogibanje nadzoru svetlobe in temperature med shranjevanjem in transportom, kot je uporaba rjavih steklenic in njihovo shranjevanje v hladnem skladišču, da preprečite nadaljnje poglabljanje barve in poslabšanje.
Topnost: spojina ima dobro topnost v običajnih organskih topilih, kot sta toluen in diklorometan, sledi načelu podobne topnosti in ima afiniteto do organskih topil zaradi hidrofobnega dela molekule; Vendar pa je topnost v vodi nizka in molekula težko učinkovito prekine močno vodikovo vez med molekulami vode, zaradi česar jo je težko razpršiti.
Vrelišče in gostota: podatki o vrelišču so tesno povezani z njegovo hlapnostjo in lahko zagotovijo ključne parametre za postopke, kot sta destilacija in čiščenje, vendar na žalost posebna vrednost vrelišča ni bila široko razkrita. Njegova gostota je nekoliko višja od gostote vode in razumevanje gostote lahko pomaga pri natančni oceni razmerja pretvorbe prostornine in mase v eksperimentalnih operacijah ali industrijskih procesih, kot sta prenos tekočin in natančno merjenje.
Kemijske lastnosti
Substitucijska reakcija: Atom klora in atom fluora v molekuli sta potencialni reaktivni mesti. Pri nukleofilni substitucijski reakciji lahko močni nukleofili napadejo mesta, kjer se nahajajo atomi klora in fluora, zamenjajo ustrezne atome in ustvarijo nove derivate piridina. Na primer, kombinirali so ga z nekaterimi nukleofili, ki vsebujejo dušik in žveplo, da bi razvili vrsto heterocikličnih spojin, ki vsebujejo dušik, s kompleksnejšo strukturo za odkrivanje zdravil ali sintezo materialov.
Redoks reakcija: sam piridinski obroč je relativno stabilen, toda ko se močni oksidanti, kot sta kalijev permanganat in vodikov peroksid, povežejo s kislimi pogoji, lahko pride do oksidacije, kar povzroči uničenje ali modifikacijo strukture piridinskega obroča; Nasprotno pa je s primernim redukcijskim sredstvom, kot so kovinski hidridi, teoretično mogoče hidrogenirati intramolekularne nenasičene vezi.
Četrtič, metoda sinteze
Običajna pot sinteze je, da začnemo s preprostimi derivati piridina in postopoma zgradimo ciljno strukturo z reakcijami halogeniranja in fluoriranja. Izhodni material piridinske spojine se najprej selektivno metilira in hkrati uvede metilne skupine; Nato uporabite reagente za halogeniranje, kot sta klor in tekoči klor, s primernimi katalizatorji in reakcijskimi pogoji, da dosežete uvedbo atomov klora; Končno so bili uporabljeni fluorirani reagenti, kot je Selectfluor, za natančno fluoriranje ciljnega mesta, da smo dobili 2-kloro-3-fluoro-6-metilpiridin.
Uporabe
Intermediati za sintezo zdravil: njegovo edinstveno strukturo obožujejo medicinski kemiki in je visokokakovosten intermediat za razvoj novih antibakterijskih, protivirusnih in protitumorskih zdravil. Elektronske lastnosti in prostorska struktura piridinskih obročev in njihovih substituentov se lahko specifično vežejo na ciljne proteine in vivo in se pričakuje, da se bodo po kasnejši večstopenjski modifikaciji spremenile v aktivne sestavine z odlično učinkovitostjo.
Znanost o materialih: Na področju sinteze organskih materialov se lahko uporablja za izdelavo funkcionalnih polimernih materialov, fluorescentnih materialov itd., na podlagi svoje sposobnosti natančne uvedbe klorovih, fluorovih atomov in piridinskih struktur ter materialom daje posebne električne in optične lastnosti. lastnosti in spodbujanje razvoja najsodobnejših tehnologij, kot so pametni materiali in zaslonski materiali.